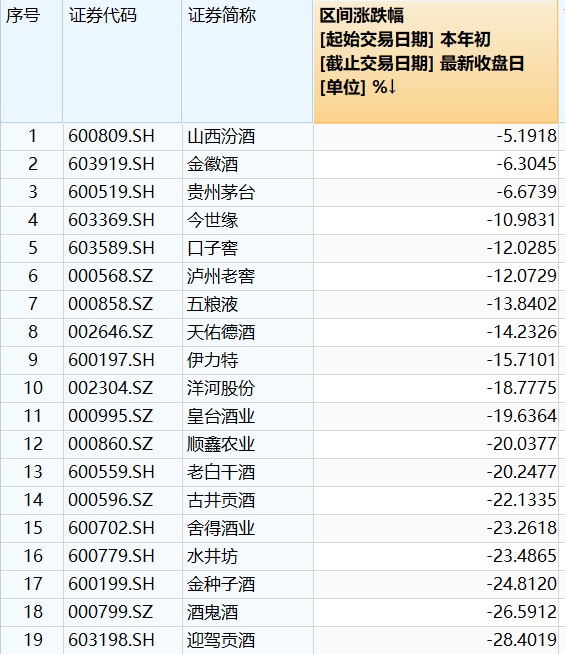
近日,国家药监局有大动作!在北京、上海等地试点差不多一年之后,又发文要明确 “纳入创新药临床试验审评审批30日通道” 的药物范畴,这可真是医药行业里一件让人特别关注的事!到底这会给咱们医药界带来啥大变化?咱们接着往下看!
试点背景情况
大概在一年前,国家就有动作了。像上海在去年7月30日发布 “关于支持生物医药产业全链条创新发展的若干意见”,推动国家改革试点,把药品补充申请审评时限压缩到60个工作日,药物临床试验申请审评审批时限压到30个工作日。北京也在同年发文,推行 “药品补充申请审评时限从200日压到60日,药品临床试验审批时限从60日到30日” 的创新试点。你瞧瞧,那时候国家就在探索提升医药发展质量和效率的办法
试行政策明确
当年国家药监局发通知明确 “探索建立全面提升药物临床试验质量和效率的工作制度和机制”,要30个工作日内完成创新药临床试验申请审评审批。并且还规定,试点项目范围是 “1类创新药(细胞和基因治疗产品、疫苗产品等除外)临床试验申请”。这都是一步步在谨慎推进,真的是费了不少心思。
审批通道优势
这次征求意见稿里讲的30日通道可厉害!它支持国家重点研发品种,鼓励全球早期同步研发和国际多中心临床试验。这就好比给咱们打开了一扇国际化的大门,能为国际多中心临床试验提供有力支持,能加速全球药物在中国市场的同步研发进程。咱也能和国际药物研发紧密结合起来,这多好
责任明确重要
征求意见稿还很明确地强调了药物临床试验申请人的主体责任。在提交申请前,人家得和药物临床试验机构合作,同步开展立项、伦理审查。还得有与申报品种研发风险相适应的评估和管理能力,而且得承诺获批后12周内启动临床试验。这么做也是为了让整个过程更严谨,不能出啥岔子,这可是为了大众用药安全着想。
国内药企机遇
这一系列政策对咱国内药企简直是大大的机遇审批时间缩短,能让药企的创新药更快地上路。药企可以更快开展临床试验,加速新药上市进程,这对于药企来讲,那就是提高竞争力,获得更多生存和发展机会。这就激励着药企大胆创新研发官渡第五中学,为咱们国内的医药事业做更多贡献!
大众用药利好
对咱老百姓来说,这可是特大的利好这样一来,新药能更快上市。咱以后在面对各种各样疾病的时候,就能有更多更新更有效的药物可以选择。这要是真能不断推进,没准以后很多疑难病症都能被更快攻克,就会少受很多病痛的折磨
你说,国家这样一步步推进试点,不断细化政策,这药物审评审批30日通道之后到底还会有啥具体的好效果?